Saber identificar signos de dolor en animales exóticos es crucial para preservar su bienestar animal y cumplir con nuestro deber como veterinarios. Sin embargo, a veces puede ser difícil identificar el dolor en nuestros pacientes exóticos, especialmente en aquellos que ocultan signos de dolor y enfermedad como mecanismo de protección frente a los depredadores.

Los animales exóticos tienen formas únicas de expresar y ocultar el dolor y es nuestro deber saber identificarlo. Dependiendo de la especie, los signos de dolor pueden ser sutiles o incluso estar completamente ocultos. Es importante recordar que todos los animales exóticos sienten dolor. Por lo tanto, debemos asumir que las condiciones consideradas dolorosas en un paciente canino o felino también lo serán para un paciente exótico y tratarlos en consecuencia(Figura 1).
Pequeños mamíferos
Reconocer el dolor en los pequeños mamíferos
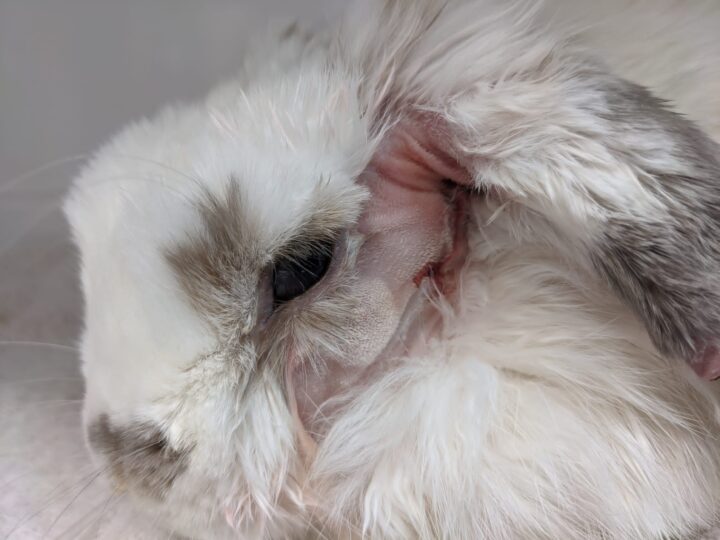
Los pequeños mamíferos suelen ser los más fáciles de evaluar a la hora de identificar dolor. Estos incluyen aumento de las contracciones, tensión orbital(Figura 2), arqueamiento de la espalda(Figura 3), presión abdominal, aplanamiento de la nariz o las mejillas y piloerección (Malik y Leach, 2017).
Se han desarrollado varias escalas de dolor para evaluar los signos visibles en conejos (Keating et al., 2012), ratas (Sotocina et al., 2011) y ratones (Langford et al., 2010). Estas "escalas de muecas" utilizan identificadores visuales del dolor para asignar un nivel de dolor o puntuación numérica que puede ser vital para garantizar que un paciente reciba un nivel aceptable de analgesia.

Al evaluar los signos de dolor en estos pacientes, es fundamental observarlos en un estado lo más tranquilo y natural posible, con el fin de identificar con precisión cualquier cambio apreciable (Flecknell, 2018). Se ha demostrado que los distintos tipos de dolor se manifiestan de manera diferente en los pequeños mamíferos. Por ejemplo, el dolor visceral suele identificarse por la presión en el vientre, el tambaleo, un aspecto ahuecado de los flancos en cobayas y una postura arqueada de la columna vertebral en ratas (Flecknell, 2018).
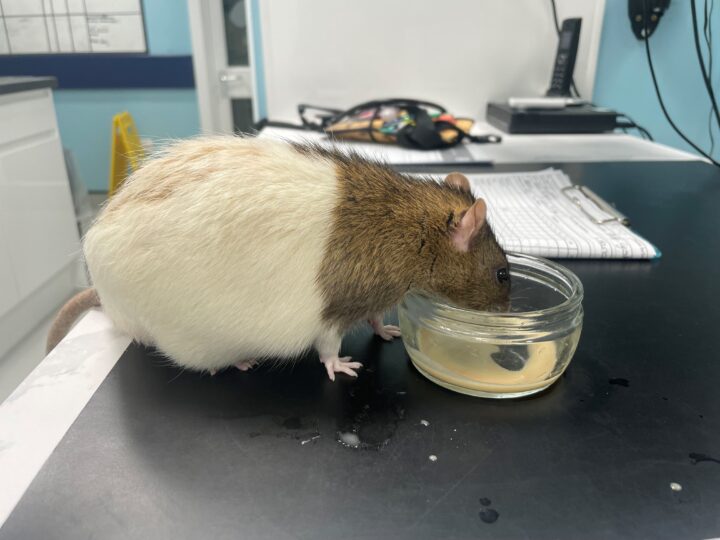
Los signos de comportamiento también pueden utilizarse para identificar signos de dolor en pequeños mamíferos. La disminución de los comportamientos de acicalamiento, la disminución de la alimentación, la inquietud y los cambios de temperamento son signos de dolor observados con frecuencia en pacientes de pequeños mamíferos (van Zeeland y Schoemaker, 2023)(Figura 4).
Si existe cualquier duda de que el paciente esté sufriendo dolor, se debe administrar analgesia sin demora.
Recientemente se han desarrollado escalas de dolor, como la Bristol Rabbit Pain Scale (Benato et al., 2023), que permite, tanto a los profesionales veterinarios como a los propietarios, evaluar los comportamientos de los pequeños mamíferos y asignar una puntuación numérica para determinar si el paciente sufre dolor o no. Es importante recordar que todas las escalas de dolor son subjetivas, ya se basen en identificadores visuales o en comportamientos identificados. Esto significa que dos evaluadores a los que se les presente el mismo paciente al mismo tiempo pueden puntuar de forma diferente dependiendo de la interpretación de la escala. Estas escalas ayudan a guiarse pero el paciente debe evaluarse siempre en su totalidad.
Tratamiento del dolor en pequeños mamíferos
Las opciones de analgesia en pequeños mamíferos son amplias. Dependiendo de la especie y del fármaco evaluado, existen muchos estudios de eficacia para diferentes clases de analgesia en estas especies. Un amplio formulario de animales exóticos es ideal para acceder a las referencias de estos estudios y sus tasas de dosis asociadas (Carpenter y Harms, 2023). Los pequeños mamíferos suelen requerir dosis mucho más altas de fármacos analgésicos de uso común y a intervalos más regulares que los pacientes caninos y felinos, por lo que es importante consultar un formulario antes de prescribir.
Se recomienda la analgesia multimodal y, si es posible, la analgesia debe administrarse antes del estímulo doloroso (por ejemplo, antes de la cirugía). Existen diversas opciones y entre ellas se incluyen opioides, antiinflamatorios no esteroideos (AINE), anestesia local (administrada por vía tópica o intravenosa), gabapentina, paracetamol, ketamina y tramadol. En particular, la analgesia debe utilizarse ampliamente en los fermentadores del intestino posterior, ya que el dolor es una causa bien conocida de estasis gastrointestinal.

Aves
Reconocer el dolor en pacientes aviares
Los signos de dolor pueden ser más sutiles en las aves que en los pequeños mamíferos, y los casos sutiles pueden requerir a menudo una persona familiarizada con los comportamientos normales de la especie presentada.
Las aves suelen ocultar signos de dolor para evitar la depredación, pero también para enmascarar signos de inferioridad respecto a otras aves de la misma especie (Douglas et al., 2018). Los signos de dolor comúnmente observados en las aves incluyen una postura encorvada, letargo, piloerección de las plumas, ojos cerrados, mal aspecto de las plumas y abdomen recogido (Paul-Murphy y Hawkins, 2015)(Figura 5). Las lesiones de las extremidades pélvicas pueden provocar cojera, dificultad para posarse o tropiezos; por su parte, las lesiones de las extremidades pectorales pueden presentarse como una caída del ala o un desplume de las plumas sobre la zona afectada (Malik y Valentine, 2017).
También pueden observarse cambios de comportamiento como agresividad en pacientes que previamente no han sido agresivos o comportamientos sumisos en animales previamente agresivos. El arrancado de plumas puede dar pistas sobre el origen del dolor, ya que algunas aves se arrancan las plumas sobre una zona de dolor o malestar. Sin embargo, esto debe observarse con precaución, ya que el arrancado de plumas es un problema multifactorial y en estos casos puede producirse una interpretación errónea de los signos.

Tratamiento del dolor en pacientes aviares
A menudo, los veterinarios no saben por dónde empezar cuando administran analgesia a pacientes aviares. Su anatomía y fisiología distan mucho de las de los mamíferos, y a menudo requieren diferentes clases de fármacos y dosis mucho más altas. Históricamente, se ha informado de que la mayoría de los pacientes aviares tienen una mayor proporción de receptores opioides kappa en comparación con los receptores opioides mu y, como resultado, el butorfanol se ha recomendado durante mucho tiempo para la analgesia en pacientes aviares. Sin embargo, investigaciones más recientes han revelado que esto no es así en todas las aves y que la distribución de los receptores opioides difiere enormemente entre especies (Fousse et al., 2020), lo que repercute en la eficacia de la analgesia opioide entre especies aviares.
Investigaciones recientes han identificado que la distribución de los receptores opioides difiere considerablemente entre especies, lo que tiene implicaciones para la eficacia de la analgesia opioide.
Por ejemplo, se ha demostrado que los cernícalos americanos muestran un aumento dependiente de la dosis en los tiempos de abstinencia térmica cuando se les administra hidromorfona por vía intramuscular (Guzman et al., 2013). Sin embargo, cuando se administró fentanilo por vía intramuscular a cacatúas paraguas, no se observó un aumento de los tiempos de abstinencia térmica hasta que se administró a las aves una dosis 10 veces superior a la suministrada a pacientes caninos y felinos, que también se asoció a una hiperactividad significativa (Hoppes et al., 2003). Se ha demostrado que la buprenorfina proporciona analgesia en cernícalos americanos a dosis de 0,1 a 0,6mg/kg (Ceulemans et al., 2014); sin embargo, dosis similares no proporcionaron un efecto analgésico en loros grises africanos (Paul-Murphy et al., 1999).
Se dispone de estudios sobre muchos agentes analgésicos diferentes para varias especies y órdenes de aves. El tramadol ha demostrado ser un analgésico eficaz en muchos órdenes de aves, al igual que varios AINE, incluido el meloxicam. Sin embargo, las dosis suelen aumentar drásticamente en comparación con las de los pacientes caninos y felinos. Por ejemplo, el tramadol requirió dosis de 30 mg/kg para alcanzar niveles plasmáticos terapéuticos en loros amazónicos hispanos (Souza et al ., 2012), y se necesitaron dosis de meloxicam de hasta 2 mg/kg en palomas para la analgesia postoperatoria (Desmarchelier et al., 2012).
La analgesia multimodal también debe utilizarse en pacientes aviares, y el uso de anestesia local para infiltración o bloqueos nerviosos puede ser un complemento útil de la analgesia oral o inyectable.
Reptiles
Reconocer el dolor en los reptiles
Los reptiles son, con diferencia, los más difíciles de evaluar. Los estudios sobre el dolor suelen ser escasos y existen grandes diferencias anatómicas y fisiológicas entre los distintos órdenes de reptiles, así como en su percepción del dolor. Por ejemplo, mientras que un estímulo térmico de retirada provoca una respuesta rápida en los mamíferos y los pacientes aviares se retiran ante un estímulo caliente, se sabe que los reptiles sufren quemaduras térmicas graves al permanecer sentados sobre elementos calientes durante horas.

FIGURA (6) Un geco leopardo mostrando una postura encorvada indicativa de dolor al día siguiente de una laparotomía exploratoria y ovariohisterectomía, justo antes de que se le administrara un opioide mu puro
Se han descrito varios signos de dolor en reptiles como la disminución de la interacción con el entorno, la disminución del apetito, la disminución de la amplitud de movimiento en las extremidades lesionadas, la alteración de los comportamientos de asoleamiento, la agresividad y los cambios de color de la piel en los lagartos que son capaces de este comportamiento (Latney, 2023). Los signos físicos manifiestos son poco frecuentes en los reptiles en comparación con otras especies exóticas, pero pueden incluir entrecerrar los ojos y una postura encorvada, espalda arqueada o cojera(Figura 6).
Tratamiento del dolor en reptiles
Hay pocos datos sobre la administración de analgésicos a los reptiles, y los estudios que demuestran su eficacia son escasos.
Algunas de las consideraciones más importantes para proporcionar analgesia son las diferencias entre especies, la temperatura del paciente y su zona de temperatura óptima preferida, a qué temperatura metabolizará mejor los fármacos, y la presencia de un sistema portal renal, que afecta al lugar donde pueden administrarse los fármacos (Mosley, 2011). Se recomienda que cualquier fármaco inyectable se administre cranealmente a los riñones para reducir los efectos del metabolismo de primer paso. La vía de administración también es importante, ya que puede afectar a la biodisponibilidad de los fármacos. Por ejemplo, el ketoprofeno administrado a iguanas verdes tuvo una reducción del 28% en la biodisponibilidad cuando se administró por vía intramuscular en comparación con la vía intravenosa (Tuttle et al., 2006).
Algunas de las consideraciones más importantes para proporcionar analgesia en reptiles son las diferencias entre especies, la temperatura del paciente y su zona de temperatura óptima preferida —a la que metabolizará mejor los fármacos—, así como la presencia de un sistema porta renal.
Las tres clases principales de fármacos analgésicos administrados a los reptiles incluyen los opioides, los AINE y los anestésicos locales. En general, se ha demostrado que los fármacos opioides mu puros proporcionan una analgesia eficaz para la mayoría de los pacientes reptiles (Sladky, 2023). La morfina ha demostrado ser eficaz para la analgesia en algunas especies de reptiles, mientras que la buprenorfina y el butorfanol no han logrado proporcionar una analgesia fiable en pacientes reptiles (Mosley, 2011). Se ha demostrado que el tramadol proporciona analgesia duradera en quelonios y lagartos durante hasta 96 horas en algunos casos (Cummings et al., 2009). La eficacia de los AINE en reptiles es difícil de interpretar, ya que las respuestas al dolor son difíciles de medir y la medición de las concentraciones plasmáticas no siempre se correlaciona con las concentraciones tisulares o la eficacia garantizada. La anestesia local puede utilizarse en pacientes reptiles, describiéndose protocolos de bloqueo local, bloqueo nervioso e incluso epidural (Sladky, 2023).
En los reptiles se preconiza la analgesia multimodal, ya que el conocimiento de agentes analgésicos eficaces es escaso en este momento.
Conclusión
Reconocer el dolor en animales exóticos puede ser difícil, incluso con el uso de escalas de dolor verificadas. Es importante extrapolar los conocimientos de otras especies y considerar que un paciente exótico puede tener dolor a pesar de la ausencia de signos clínicos. Los fármacos analgésicos de uso común en la práctica de los animales de compañía pueden utilizarse en todas las especies exóticas; sin embargo, debe consultarse primero un formulario completo, ya que las dosis y los intervalos de dosis pueden variar drásticamente entre especies y algunos fármacos pueden carecer de eficacia en algunas especies, en particular las especies de reptiles.





