Les chats diabétiques peuvent être difficiles à gérer. Nous savons que le suivi de la réponse à l’insuline et la prévention de l’hyper- et de l’hypoglycémie sont essentiels pour contrôler efficacement les signes cliniques. Cependant, les courbes de glycémie peuvent être affectées par le stress en clinique (Sparkes et al., 2015), et la prise répétée d’échantillons sanguins peut générer du stress et des associations négatives. Parmi les alternatives, on trouve la mesure de la glycémie à domicile par des propriétaires volontaires (Hazuchova et al., 2017). Même si cette méthode est souvent efficace, des variations quotidiennes dans les courbes peuvent influencer les décisions thérapeutiques (Alt et al., 2007).
Les moniteurs de glycémie en continu (CGM) sont de plus en plus utilisés en médecine des petits animaux pour surveiller les patients diabétiques, qu’ils soient chiens ou chats. Ils semblent offrir une solution aux limites des courbes de glycémie ponctuelles et permettent d’éviter les multiples ponctions veineuses. Ces dispositifs sont généralement bien tolérés et faciles à installer, et des études récentes ont montré qu’ils peuvent jouer un rôle important dans la gestion du diabète félin. Cet article passe en revue ces preuves, décrit la procédure d’installation, aborde les complications possibles et explique dans quelles situations un tel dispositif peut être le plus bénéfique pour le patient félin diabétique.
À propos des systèmes de surveillance du glucose en continu

Le système de surveillance continue de la glycémie (CGM) le plus couramment utilisé actuellement est le FreeStyle Libre (Abbott), constitué d’un petit capteur en forme de disque placé sur l’animal (Figure 1), qui mesure le glucose interstitiel et fonctionne soit avec une application pour téléphone mobile, soit avec un dispositif de lecture qui stocke les données du capteur. En plus de fournir une valeur glycémique, le téléphone ou le lecteur affiche une flèche indiquant si le glucose interstitiel est en train d’augmenter ou de diminuer. Contrairement aux systèmes précédents, l’appareil n’a pas besoin d’être calibré avec la glycémie et peut mesurer pendant 14 jours, bien que la durée puisse être plus courte chez les chats. Le capteur peut stocker jusqu’à huit heures de données, qui sont ensuite facilement transférées vers le téléphone ou le lecteur.
La précision du FreeStyle Libre a été évaluée chez l’humain, se comparant favorablement à la glycémie capillaire. Trois études récentes chez le chat ont également montré une bonne concordance entre les mesures de glucose interstitiel et de glucose sanguin (Deiting et Mischke, 2021 ; Del Baldo et al., 2021 ; Shea et Hess, 2021). Cependant, le délai d’équilibrage entre le sang et l’interstitium doit être pris en compte en cas de divergences entre les résultats. Del Baldo et al. (2021) ont montré que lors de variations rapides de la glycémie, des différences marquées peuvent apparaître entre les deux compartiments, ce qui doit être considéré lors de l’interprétation des données. Deiting et Mischke (2021) ont également observé que certaines lectures différaient significativement entre le glucose interstitiel et le glucose sanguin, en particulier chez certains patients.
Tous les résultats non plausibles doivent être vérifiés par une mesure de la glycémie sanguine, et les tendances doivent être analysées en tenant compte des limites de l’appareil. Le système a été conçu pour les patients humains diabétiques et dispose donc de paramètres prédéfinis pour cette espèce.
Le système a été conçu pour les patients humains diabétiques et dispose donc de paramètres prédéfinis pour cette espèce. Le système Libre 2 permet de déclencher une alarme lorsque le glucose interstitiel dépasse ou descend en dessous de certains seuils, bien que cette fonction puisse être désactivée.
Application du dispositif
La grande majorité des capteurs peuvent être posés sur des patients conscients, mais l’installation du capteur nécessite une légère pression. Pour certains patients félins, notamment ceux qui ne sont pas habitués à la pose de capteurs, une sédation ou une anxiolyse à l’aide de gabapentine ou de butorphanol peut être utile. Si les patients diabétiques sont déjà sédatés pour d’autres procédures (par exemple pour l’imagerie), il est recommandé de profiter de l’occasion pour placer le capteur. Chaque capteur est fourni avec un applicateur (Figure 2), nécessaire pour installer correctement le disque du capteur.
Le dispositif peut être placé à différents endroits, et plusieurs études ont exploré différents sites. Chez le chat, le cou dorsal peut être utilisé (Shea et Hess, 2021), ou bien le thorax dorsal, caudal à l’omoplate (Figure 3 ; Deiting et Mischke, 2021 ; Shoelson et al., 2021). Il est important de raser soigneusement la zone, de la nettoyer pour enlever toute saleté (des lingettes sont fournies avec le capteur) et de la laisser sécher complètement avant la pose du capteur.
Bien que le disque du capteur soit adhésif, l’auteur ajoute parfois des « points » de colle tissulaire (cyanoacrylate) autour du bord de la zone adhésive, car les bords peuvent se détacher avec le temps (Figure 4). Cette stratégie a également été adoptée dans des études récentes (Del Baldo et al., 2021 ; Shea et Hess, 2021). Dans une étude portant sur 34 chats diabétiques, les auteurs n’ont pas utilisé d’adhésif supplémentaire, mais ont fixé les bords avec des sutures, ce qui a été bien toléré (Deiting et Mischke, 2021). D’après l’expérience de l’auteur, cette étape n’est pas systématiquement nécessaire.




L'interférence du patient est rare et, en général, il n'est pas nécessaire de recouvrir le capteur. Chez les chats, les pansements et les t-shirts provoquent du stress, limitent les comportements naturels et peuvent influencer les relevés. Si le capteur est placé sur le cou, certains cliniciens choisissent de le recouvrir d’un pansement lâche ou d’un collier en tissu (Del Baldo et al., 2021). Dans la clinique de l’auteur, un collier Buster souple est utilisé pour protéger le capteur chez les chats.
Il peut être utile d’envisager une sédation légère si le patient est anxieux ou si vous n’êtes pas familier avec la pose du capteur, car elle peut être un peu délicate au début. La gabapentine (administrée deux heures avant l’application) ou le butorphanol (30 minutes avant l’application) peut suffire.
|
Interprétation des données
Le capteur doit être scanné toutes les huit heures pour transférer les données vers un téléphone ou un lecteur. Les clients peuvent ensuite envoyer les résultats à la clinique via l’application, ou connecter le lecteur à un ordinateur pour télécharger les données après avoir installé le logiciel requis.
La Figure 6 présente un exemple de rapport, comprenant plusieurs éléments : des graphiques journaliers, la glycémie moyenne quotidienne et le pourcentage de temps pendant lequel le glucose interstitiel se situe dans certaines plages prédéfinies (celles-ci étant basées sur les valeurs humaines). Parmi toutes les informations obtenues, les graphiques sont généralement les plus utiles pour le suivi.
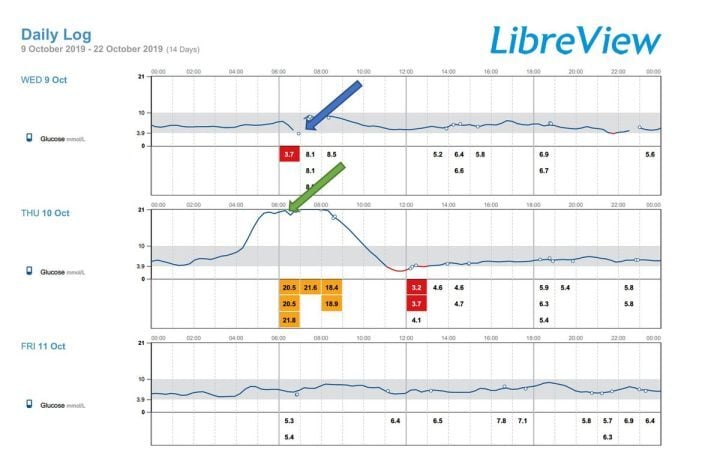
Ce chat est en phase de rémission. Une hypoglycémie est observée au jour 1 (flèche bleue), tandis qu’une période d’hyperglycémie apparaît au jour 2 (flèche verte), coïncidant avec un déplacement à la clinique. Cela illustre l’effet du stress sur la glycémie et montre comment les décisions basées sur ces lectures peuvent conduire à une augmentation de la dose d’insuline.
Dans ce contexte, le CGM est particulièrement utile pour visualiser les mesures effectuées à domicile sur une période prolongée, offrant une vue d’ensemble plus complète de l’état du patient.
Indications pour l'utilisation d'un CGM
Le système peut être utilisé en clinique chez les chats récemment diagnostiqués afin de vérifier leur réponse à l’insuline et la durée de son effet. Une fois cette évaluation réalisée, le patient peut quitter l’hôpital avec le capteur en place. Les chats atteints d’acidocétose diabétique (ACD), les diabétiques instables (par exemple, ceux présentant des signes cliniques persistants, des épisodes récurrents d’hyperglycémie ou d’hypoglycémie, ou une suspicion d’effet Somogyi), ainsi que les patients félins proches de la rémission, peuvent également bénéficier de l’utilisation de ce système.
Le CGM peut également être utilisé chez les patients septiques ou en état critique, chez lesquels l’hypoglycémie représente un risque, ainsi que chez ceux recevant une perfusion continue d’insuline ou de glucose. Cependant, ces indications n’ont pas encore été étudiées chez les chats. Il convient également de prendre en compte le décalage entre le glucose sanguin et le glucose interstitiel, particulièrement marqué lors de variations rapides de la glycémie (Del Baldo et al., 2021).
Pour ces patients, il est recommandé de valider les résultats du CGM par des mesures classiques de glycémie avant d’ajuster les protocoles de traitement.
L’auteur a constaté que [un CGM] est particulièrement utile chez les chats en voie de rémission, chez les patients atteints d’acidocétose diabétique (ACD) et chez les animaux pour lesquels le stress en clinique est très susceptible d’influencer l’interprétation de la courbe glycémique et les décisions concernant la dose d’insuline.
L'auteur a trouvé cette méthode très utile chez les chats en voie de rémission, chez les patients atteints d'ACD et chez les animaux pour lesquels le stress de la clinique est susceptible d'influencer l'interprétation de la courbe de glycémie et les décisions relatives à la dose d'insuline. La Figure 6 montre les données d'un appareil FreeStyle Libre sur un chat entrant en rémission diabétique.
Complications et limites
Une étude récente a examiné les complications du dispositif FreeStyle Libre chez 20 chats (Shoelson et al., 2021). Au total, 33 capteurs ont été placés, la plupart sur le thorax dorsolatéral. Les complications les plus fréquentes étaient un détachement précoce du capteur (15 %) et d'autres complications liées au site cutané où le capteur est fixé, principalement une irritation mineure de la peau, deux chats ont présenté une érosion ou un abcès. Les auteurs de cette étude ont estimé qu'une application supplémentaire de colle cyanoacrylate sur la surface du capteur faisant face à la peau aurait pu contribuer au traumatisme cutané, en particulier si le capteur est ensuite retiré prématurément. Il semble judicieux de faire preuve de prudence quant à la quantité de colle utilisée. Shea et Hess (2021) ont utilisé de petites quantités de colle cyanoacrylate et ont constaté une irritation cutanée minime.
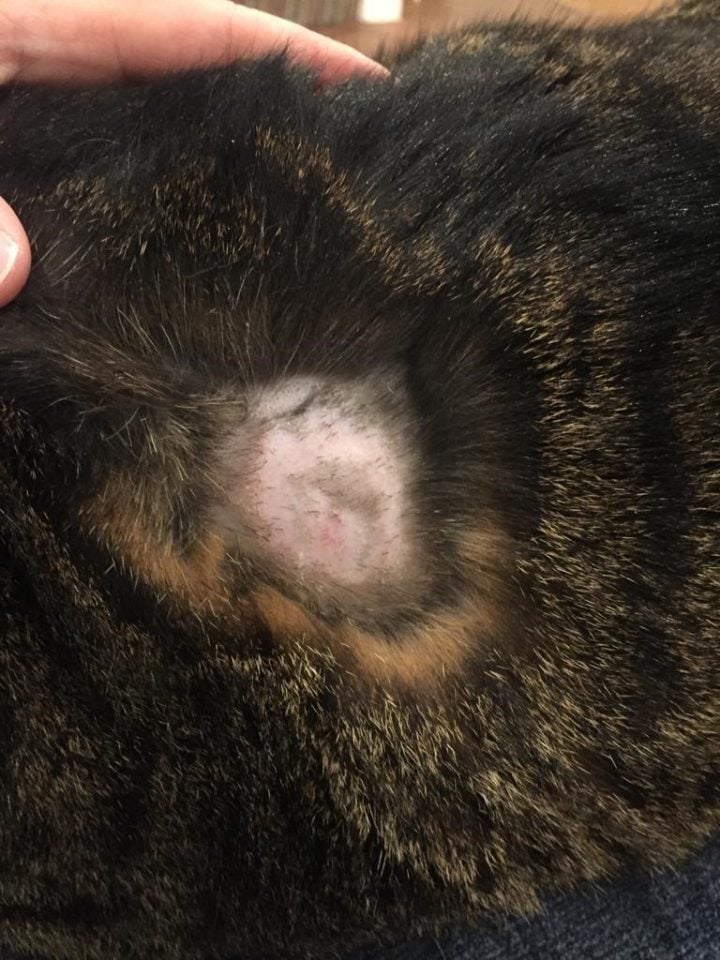
Les poils peuvent être lents à repousser dans la zone où le capteur a été placé (Figure 7), et chez les chats, la zone peut repousser avec des poils d'une couleur différente.
Deiting et Mischke (2021) ont observé que la durée de fonctionnement du capteur était souvent réduite chez leurs patients, en raison de détachements prématurés, avec une durée moyenne d’utilisation de 8,3 jours. Par ailleurs, dans leur étude sur des chats sortis avec des capteurs, Shea et Hess (2021) ont constaté que la durée médiane de fonctionnement était de sept jours, et que dans 80 % des cas, un déplacement ou une défaillance du capteur survenait avant la fin de la période d’étude de 13 jours. Ce taux élevé de défaillances pourrait être lié au positionnement du capteur, tous placés sur le cou dorsal. Cela suggère que le taux de détachement plus faible observé dans l’étude de Shoelson (15 %) pourrait résulter d’un placement sur le thorax latéral (Shoelson et al., 2021).
Les capteurs sont conçus pour la peau humaine et, chez l’homme, différents pansements et bandes permettent de les maintenir en place. Chez les chats, cependant, la peau est fine et les animaux très mobiles, ce qui peut facilement provoquer le délogement du petit cathéter, notamment chez les patients affaiblis. Dans les jours qui suivent la pose, la repousse des poils peut également décoller l’adhésif. Les propriétaires doivent être informés qu’un détachement prématuré du capteur peut survenir et que les coûts liés à cette complication et au remplacement du capteur doivent être pris en compte.
Le système CGM FreeStyle Libre a une limite supérieure de mesure du glucose interstitiel de 27,8 mmol/l et les lectures supérieures à ce niveau sont enregistrées comme "Hi". C'est potentiellement une limitation chez les chats atteints d'ACD, par exemple, car ils peuvent être extrêmement hyperglycémiques, et aussi chez les chats mal contrôlés pour lesquels cette information supplémentaire pourrait être utile.
Conclusions
Les données doivent être interprétées en tenant compte des paramètres cliniques indiquant la réponse du patient (poids, consommation d’eau, appétit), tout en reconnaissant les limites du système de surveillance.
Le CGM peut être un outil utile dans la gestion des chats diabétiques. Cependant, les données doivent être interprétées en même temps que les paramètres cliniques indiquant la réponse (poids, consommation d'eau, appétit) et les limites du système de surveillance doivent être prises en compte. Il peut y avoir une divergence entre la glycémie interstitielle et la glycémie sanguine, en particulier lors de variations rapides de la glycémie, lorsqu'un décalage temporel entre les deux compartiments peut se produire. Le capteur FreeStyle Libre a récemment été étudié chez des chats diabétiques et s’est montré bien toléré, avec une bonne précision. Cependant, le délogement prématuré du capteur est fréquent, et la durée de fonctionnement effective sera probablement inférieure aux 14 jours observés chez l’homme.
Références (cliquer pour agrandir)
_OL_CourseThumb-1.jpg?width=500&height=300&name=IVE_GPCert(SAM)_OL_CourseThumb-1.jpg)




